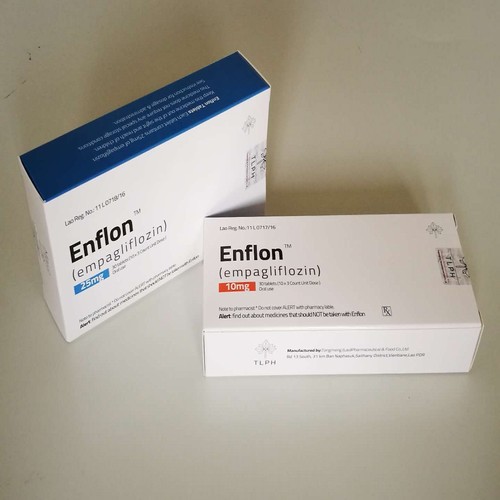
恩格列净(Empagliflozin)是一种用于治疗2型糖尿病的药物,它通过抑制肾脏中的钠-葡萄糖共转运体2(SGLT2)来减少血糖水平。该药物在国际市场上已经取得了很大的成功,并被广泛应用于糖尿病患者的治疗中。那么,恩格列净何时将在国内上市呢?下面将就这一话题进行详细介绍。
1. 国内临床研究:寻找适应症
在引入国内市场之前,恩格列净需要通过国内临床试验来评估其在中国患者中的疗效和安全性。这些试验通常包括大规模的多中心随机对照试验,涉及到不同年龄、性别和糖尿病程度的患者群体。此外,临床研究还会评估恩格列净在降低心血管风险和肾脏保护方面的潜力。
2. 安全性评估和监管审批
一旦国内的临床试验完成,研究结果需要进行安全性评估,并提交给卫生部门以获得批准。中国国家药品监督管理局(NMPA)负责监管和审批药物上市,他们在评估药物的疗效和安全性方面非常谨慎。从临床试验数据到药物注册申请,这个过程可能需要一定的时间来确保药物的质量和有效性。
3. 上市前的市场准备
在上市之前,恩格列净的生产商通常会进行市场准备工作。这包括与医疗保险公司进行谈判,以确保患者能够获得药物的报销。同时,他们还会与医疗机构和医生进行沟通,以提供关于恩格列净的信息和培训,确保其正确的使用和管理。
4. 上市时间预测
考虑到上述过程的复杂性和时间消耗,恩格列净的国内上市时间可能会有所推迟。最初,可能需要几年的时间来完成临床研究和监管审批。具体的时间表受到多种因素的影响,如国内研究的进展、监管机构的决策和制度变化等。
恩格列净是一种被广泛应用于2型糖尿病治疗的药物。虽然它在国际市场上取得了成功,但其国内上市还需经历临床研究、监管审批和市场准备等阶段。预计将会在未来几年内,在经过严格的评估和审批后,恩格列净才会在中国市场上正式上市,帮助更多的糖尿病患者控制血糖水平,提升生活质量。