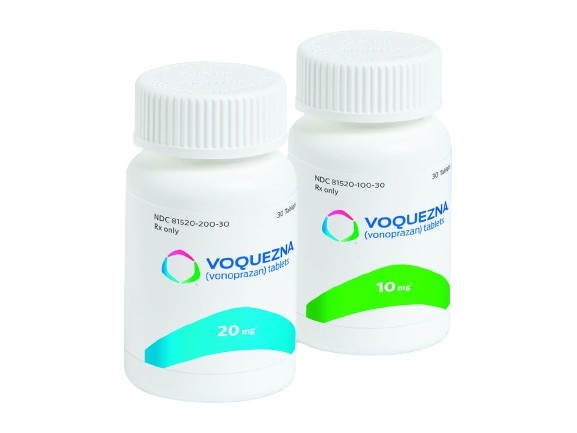
vonoprazan国内有没有上市,vonoprazan(vonoprazan)的上市时间是在2023年11月。当时,美国食品药品监督管理局(FDA)批准了Voquezna片剂用于治疗所有级别的糜烂性食管炎,以及维持所有级别糜烂性胃食管反流病(GERD)的愈合,并缓解与糜烂性GERD相关的胃灼热。
伏诺拉生(vonoprazan)是一种用于治愈各种程度的侵蚀性食管炎并缓解成人侵蚀性食管炎相关的胃灼热的药物。随着其在全球范围内的广泛应用,有关它在国内的上市情况备受关注。我们将对伏诺拉生在国内的上市情况进行调查。
1. 国内上市情况概览
截至目前,伏诺拉生在国内尚未获得上市许可。尽管伏诺拉生在一些国外市场取得了成功,但在国内的立法程序、药监局审批过程以及相关标准的要求,使得这一药物的上市进程相对较慢。许多医药公司正在与相关机构合作,积极推动伏诺拉生在国内的审批和上市。
2. 上市前的审批流程
在国内将药物引入市场之前,需要经历一系列复杂且严格的审批程序。首先,药物公司需要向国内的药监局递交申请文件,包括药物的研究数据、临床试验结果以及制造和质控相关的信息,以证明药物的质量和有效性。之后,药监局将对申请进行评估和审批,确保药物的安全性和可行性。这一过程可能需要经历多轮的交流和修改,直至达到国内药物上市标准。
3. 潜在的临床应用及益处
伏诺拉生作为一种质子泵抑制剂,是目前比较新颖的药物。它在治疗侵蚀性食管炎方面展现了良好的效果,并能够缓解成人侵蚀性食管炎导致的胃灼热症状。由于其独特的作用机制和有效性,伏诺拉生在国际上已经得到广泛应用,并取得了显著的临床成果。一旦伏诺拉生在国内成功上市,将为患者提供更多选择,并有望有效改善相关疾病的治疗效果。
4. 未来发展前景
尽管伏诺拉生在国内尚未上市,但随着科技进步和医药产业的不断发展,我们对其未来的上市前景持有乐观态度。国内的药监部门也已经意识到了伏诺拉生的重要性和潜在益处,进一步推动审批和上市进程。相信随着时间的推移,伏诺拉生会逐渐走进国内市场,为患者带来更多的康复希望。
伏诺拉生作为治疗侵蚀性食管炎和缓解胃灼热的药物,在国内尚未获得上市许可。尽管如此,我们对伏诺拉生在国内的上市前景持有乐观态度,相信其将为患者提供更多的治疗选择,有效改善相关疾病的治疗效果。随着科技和医药产业的进步,伏诺拉生有望逐渐进入国内市场,为患者带来更多的康复希望。