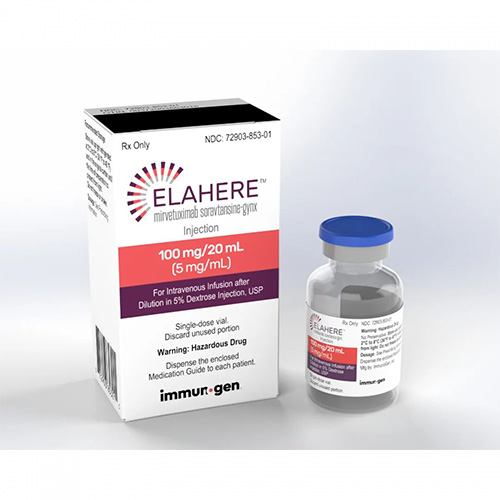
Elahere
生产厂家:美国immunomedics
功能主治:卵巢癌等总缓解率31.7%,完全缓解率4.8%
用法用量:用法用量 推荐剂量 Elahere的推荐剂量为6 mg/kg,基于调整后的理想体重(AIBW),每3周(21 天周期)静脉输注一次,直至疾病进展或出现不可接受的毒性。 Elahere 的总剂量是根据每个患者的AIBW 使用以下公式计算出来的:AIBW =理想体重(IBW [kg]) + 0.4*(实际体重[kg]-IBW) 女性 IBW(kg)= 0.9 *身高(cm)-92。 术前用药 在每次输注 Elahere 之前给予表 1 中的术前用药,以减少输注相关反应(IRRs)、恶心和呕吐的发生率和严重性。 对于出现IRRs的患者,在 Elahere 给药前一天考虑额外的术前用药,包括皮质类固醇。 眼科检查和术前用药 眼科检查:在开始 Elahere 之前,前8个周期每隔一个周期,根据临床指征进行眼科检查,包括视力和裂隙灯检查。 眼部局部类固醇:推荐使用眼部局部类固醇。 任何皮质类固醇药物的初始处方和更新应仅在用裂隙灯检查后进行。 从每次输注的前一天开始,在每只眼睛中施用一滴眼用局部类固醇,每天 6 次,直到第 4 天;然后在每个 Elahere 周期的第 5-8 天,每天 4 次,每只眼睛滴一滴眼用局部类固醇。 润滑眼药水:在使用 Elahere 治疗期间,建议每天至少使用四次润滑眼药水。 指导患者使用润滑眼药水,并建议在眼部外用类固醇给药后至少等待10分钟,再滴注润滑眼药水。 给药方法 1、 制备 1)Elahere 比较危险,应遵循适用的特殊处理和处置程序; 2)计算剂量(mg)(基于患者的 AIBW)、所需溶液的总体积(mL)和所需 Elahere 的小瓶数。 一次用药可能需要不止一瓶; 3)从冰箱中取出装有 Elahere 的小瓶,让其升温至室温; 4)注射用药品在给药前应目视检查是否有颗粒物质和变色。 Elahere 是一种澄清至略带 乳白色的无色溶液。 在抽取计算剂量的 Elahere 用于后续进一步稀释之前,轻轻旋转并检查每个小瓶。 不要摇动小瓶。 使用无菌技术,抽取计算的 Elahere 剂量体积,用于后续的进一步稀释; 5)Elahere 不含防腐剂,仅供单剂量使用。 丢弃药瓶中剩余的任何未使用的药物; 2、 稀释 1)给药前,必须用 5%葡萄糖注射液将Elahere稀释至最终浓度为1mg/mL至2mg/mL; 2) Elahere与0.9%氯化钠注射液不相容。 Elahere不得与任何其他药物或静脉注射液混合; 3)确定达到最终稀释药物浓度所需的葡萄糖注射液的体积。 从预装的静脉注射袋中取出过量的 5%葡萄糖注射液,或将计算体积的 5%葡萄糖注射液加入到无菌的空静脉注射袋中。 然后将计算好剂量体积的 Elahere 加入静脉注射袋中; 4)缓慢翻转袋子数次,轻轻混合稀释的药物溶液,以确保混合均匀。 不要摇晃或搅动; 5)如果稀释的输注液没有立即使用,将溶液在环境温度 (18℃至 25℃)下储存不超过 8 小时(包括输注时间),或者在2℃至8℃下冷藏不超过12小时。 如果冷藏,给药前让输 液袋达到室温。 冷藏后,在8小时内(包括输液时间)使用稀释的输液; 6)不要冷冻配制好的输注溶液; 3、 给药 1)给药前,目视检查Elahere 静脉输液袋是否有颗粒物质和变色; 2)在使用Elahere之前根据需要进行术前用药; 3)使用 0.2 或 0.22 um 聚醚砜(PES)在线过滤器,仅将 Elahere 作为静脉输注给药。 不要用其他膜材料替代; 4)以 1mg/min 的速度静脉输注初始剂量。 如果以 1mg/min 的速度输注 30 分钟后耐受性良好,输注速度可增加至 3mg/min。 如果以3mg/min的速度输注30分钟后耐受性良好,输注速度可增加至5mg/min; 5)如果前一剂量未发生输注相关反应,则后续输注应以最大耐受速率开始,并可增加至最大输注速率 5 mg/min(如耐受); 6)输注后,用 5%葡萄糖注射液冲洗静脉管线,以确保给予全部剂量。 不要使用任何其他静脉注射液进行冲洗;
查看详情
索米妥昔单抗(Mirvetuximab soravtansine)在国内上市了吗,索米妥昔单抗(Mirvetuximab soravtansine)于2022年11月15日在美国获得加速批准上市。目前国内未上市。
索米妥昔单抗(Mirvetuximab soravtansine)是一种针对卵巢上皮癌、输卵管癌和原发性腹膜癌的创新型抗体药物。近年来,该药物在国际上引起了广泛的关注和积极的临床研究。那么,索米妥昔单抗是否已经在国内上市呢?下面将对此进行详细探讨。
1. 索米妥昔单抗的背景与特点
索米妥昔单抗是一种人源化抗体药物,它与特定的抗体药物载体结合,并针对卵巢上皮癌、输卵管癌和原发性腹膜癌中过度表达的一种蛋白质——癌胚抗原5T4进行定向治疗。目前已有多项临床试验研究表明,该药物在治疗上述恶性肿瘤方面具有潜力。
2. 索米妥昔单抗国内临床研究进展
目前,索米妥昔单抗在中国已经进行了多项临床研究,并取得一定的研究成果。这些研究主要涵盖了药物的安全性、有效性、药代动力学以及与化疗联合应用的疗效等方面。这些研究结果显示,索米妥昔单抗在国内的临床应用前景广阔,有望为患有卵巢上皮癌、输卵管癌和原发性腹膜癌的患者带来新的治疗选择。
3. 索米妥昔单抗在国内的上市情况
截至目前,尚未有关于索米妥昔单抗在国内的上市申请获准或具体的上市日期公布。由于该药物在国际上的积极研究进展和潜力,以及中国在抗癌药物研发与上市方面的重视和加速审评的政策支持,人们对索米妥昔单抗在国内上市的期待依然很高。
4. 对索米妥昔单抗上市的期待
索米妥昔单抗作为一种新型的靶向抗癌药物,在治疗卵巢上皮癌、输卵管癌和原发性腹膜癌方面具有潜在的优势。一旦索米妥昔单抗在国内上市,将对这些肿瘤患者的治疗带来重大突破和改善。相信随着国内相关审批程序的顺利进行,索米妥昔单抗在中国的上市将会实现,并在临床实践中发挥重要作用。
索米妥昔单抗作为一种有望用于治疗卵巢上皮癌、输卵管癌和原发性腹膜癌的创新型抗体药物,尽管目前尚未在国内市场上市,但其在国内的临床研究取得了一定的进展。我们对索米妥昔单抗在中国上市的期待依然很高,相信它将为这些恶性肿瘤的治疗带来新的希望与可能。