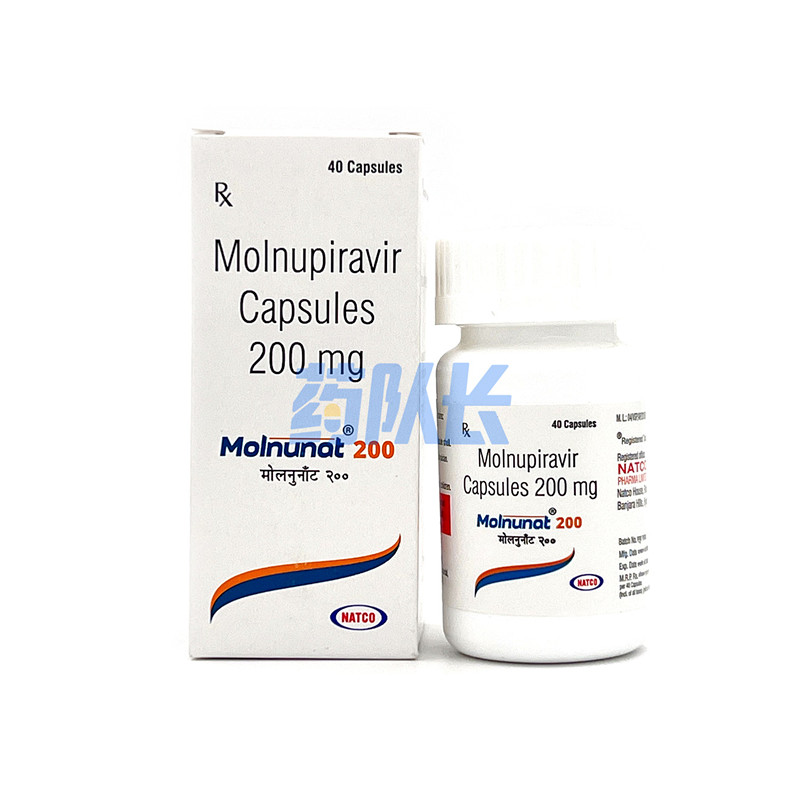
莫诺拉韦(Molnupiravir)利卓瑞国内有没有上市,莫诺拉韦(Molnupiravir)在国外最早上市的时间是2021年11月4日,首次获得批准的地点是英国。目前已经在中国上市,于2022年12月29日获得国家药品监督管理局的应急附条件批准,正式进入中国市场销售推广。2023年1月13日,该药物在中国市场首发。
随着COVID-19(新冠病毒)的全球蔓延,人们对于治疗和预防这一病毒的需求持续增加。在过去几年里,各种疫苗和药物已经问世,其中莫诺拉韦(Molnupiravir)利卓瑞备受关注。本文将探讨莫诺拉韦在国内是否已经上市,并对其可能带来的影响进行一定的讨论。
1. 莫诺拉韦药物的概述
莫诺拉韦是一种口服抗病毒药物,由Merck和Ridgeback Biotherapeutics共同开发。该药物的原理是通过干扰病毒基因的复制和传播,从而抑制病毒的增殖。初步研究表明,莫诺拉韦对抗新冠病毒具有潜在的疗效,并且可在早期感染阶段减轻病情的严重程度。
2. 莫诺拉韦的临床试验进展
莫诺拉韦的临床试验在不同国家和地区进行,以评估其对COVID-19的治疗效果和安全性。早期的研究结果显示,莫诺拉韦可以显著减少新冠毒量,并且对于高风险人群,可以降低肺炎进展为严重疾病的风险。根据相关的报道,莫诺拉韦已经取得了一定的进展,并且被某些国家批准临床使用。
3. 莫诺拉韦在国内市场的情况
截至目前,莫诺拉韦在国内尚未获得正式的上市许可。值得注意的是,莫诺拉韦已经在一些国家获得紧急使用授权或条件批准,以应对COVID-19疫情。这意味着莫诺拉韦可能在未来的时间内在国内市场获得上市许可。
4. 莫诺拉韦上市的潜在影响
如果莫诺拉韦在国内获得上市批准,将给COVID-19的治疗和控制带来重要的变化。作为一种口服药物,莫诺拉韦的使用更加方便,可以在早期感染时迅速干预,减少病毒传播和严重病情的发展。这也有助于减轻医疗资源压力,提高治疗效率。
尽管莫诺拉韦在国内尚未正式上市,但其在抗击COVID-19方面所展示的潜力无疑引起了全球的关注。随着临床试验的进展和莫诺拉韦在其他国家的批准使用,我们有理由相信,这种药物很可能在国内市场上市,并为新冠病毒的治疗和控制带来积极的影响。我们需要等待相关部门的决策和审批过程的完成,以了解莫诺拉韦在国内的最新动态。