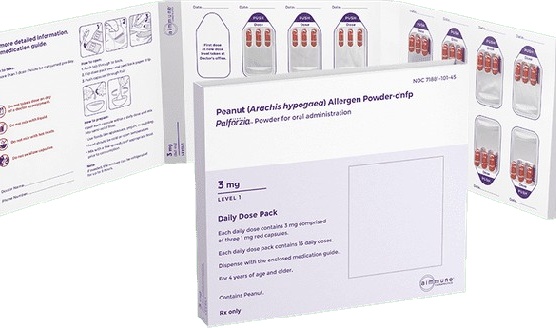
Palforzia(Peanut(Arachis hypogaea) Allergen Powder-dnfp)在国内上市了吗,Palforzia(Peanut(Arachis hypogaea) Allergen Powder-dnfp)于2020年1月31日获得美国FDA的批准上市,目前国内未上市。
近年来,Palforzia(Peanut Allergen Powder-dnfp)作为一种针对花生过敏症的新型治疗方法,在国际上引起了广泛关注。这种治疗方法通过逐步暴露患者于花生蛋白,以帮助他们逐渐建立免疫耐受。对于国内的花生过敏患者而言,他们是否能够获得这种创新治疗,却是一个备受关注的问题。
1. 国内市场现状
截至目前,Palforzia尚未在中国正式上市。尽管在国际市场上,这种治疗方法已经得到了批准并开始应用,但其在中国的注册和审批过程尚未完成。这也意味着,中国的花生过敏患者目前仍无法直接通过正规渠道获取Palforzia治疗。
2. 审批和注册进程
要在中国上市,任何新药物或治疗方法都必须经过严格的审批和注册程序。这包括安全性、有效性以及在中国患者群体中的适用性等多个方面的临床研究和数据证明。在这个过程中,制药公司需要提交大量的数据和文件,经过国家药品监督管理局(NMPA)的审查批准后,方可在中国市场上市销售。
3. 患者期待与需求
对于中国的花生过敏患者及其家庭来说,Palforzia的上市意味着一个新的治疗选择,尤其是对那些长期以来没有有效治疗方法的患者而言,这将是一个重大的进步。由于目前尚未获得国内的批准,许多患者和家属仍在等待和期待这一治疗方法能够尽快在中国推广使用。
4. 未来展望
随着全球医药研究和创新的不断发展,中国的患者通常能够从最新的治疗技术和药物中受益。希望随着Palforzia在国际上的应用和临床研究积累,它能够尽快完成在中国的注册审批,为更多的花生过敏患者带来新的希望和治疗选择。
综上所述,虽然Palforzia(Peanut Allergen Powder-dnfp)在国际上已有应用,但在中国市场上市仍面临审批和注册等多重挑战。花生过敏患者和其家庭需求这种新型治疗方法的呼声日益高涨,期待它早日在中国落地生根,造福更多有需要的患者。