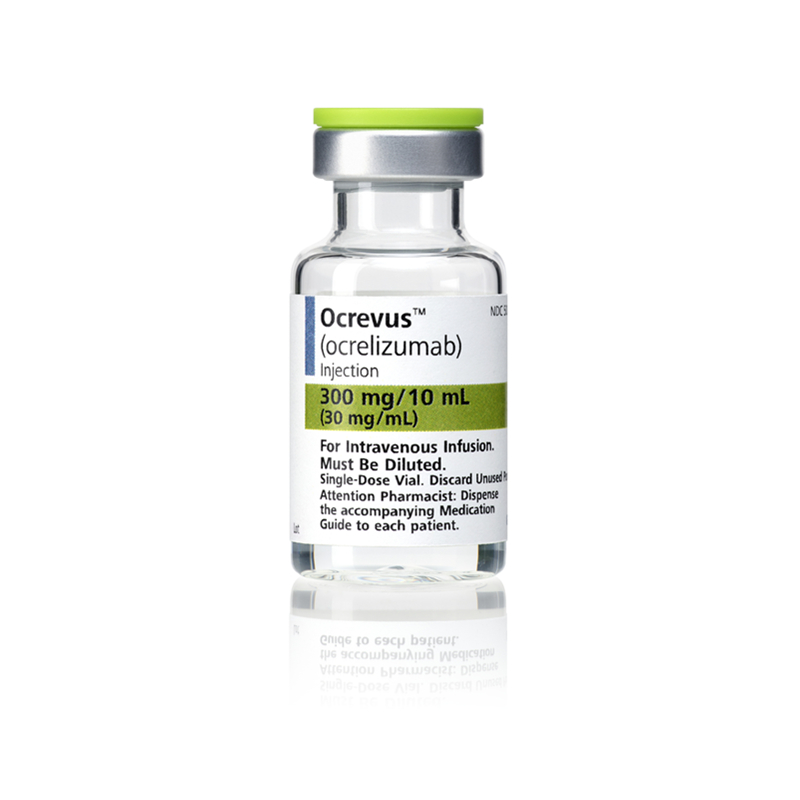
奥瑞珠单抗(Ocrelizumab)在国内上市了吗,奥瑞珠单抗(Ocrelizumab)美国上市时间:2017年3月28日;目前国内未上市。
奥瑞珠单抗是一种针对多发性硬化症的靶向治疗药物,近年来在国际上取得了显著的治疗效果和临床应用。但是,对于国内患者而言,能否获得这一先进治疗方式却是一个关注的焦点。究竟奥瑞珠单抗在中国市场上有无踪迹?以下将详细介绍。
1. 奥瑞珠单抗简介
奥瑞珠单抗,又称OCR,是一种人源化的单克隆抗体,作用于B细胞表面的CD20抗原,通过选择性地清除CD20阳性的B细胞,从而抑制多发性硬化症的病情进展。这种药物已经在一些国家被批准用于治疗多发性硬化症的不同类型,被视为一种重要的治疗选择。
2. 国内临床研究和应用现状
尽管奥瑞珠单抗在国际上取得了显著成就,但在中国,其临床研究和应用仍处于较为初步的阶段。国内一些医疗机构和研究中心在过去几年开展了少量的临床试验,以评估奥瑞珠单抗在中国人群中的安全性和有效性。这些研究为进一步推广奥瑞珠单抗提供了基础数据,其在国内的正式上市仍有一定距离。
3. 上市前景和挑战
尽管奥瑞珠单抗在国际上被认可为多发性硬化症治疗的创新药物,但其在中国的上市面临诸多挑战。首先是注册和批准的时间和程序,需要通过严格的药物审批流程,包括临床试验的扩展和本地化数据的提交。其次是市场准入后的定价问题,如何在保障患者可及性的前提下,确保药品的可持续供应和质量。
4. 患者期待与未来展望
随着多发性硬化症治疗需求的增加,国内患者和医疗专家对奥瑞珠单抗的期待也在逐渐增加。希望未来能够通过更多的临床研究和政策支持,使奥瑞珠单抗早日进入中国市场,为患者提供更有效的治疗选择。
综上所述,奥瑞珠单抗作为一种创新的多发性硬化症治疗药物,尚未在国内正式上市,但在临床研究和市场准入方面正逐步推进。未来随着科研和政策的进展,相信其在中国的应用和推广将会迎来更加积极的局面,为广大多发性硬化症患者带来新的希望和治疗选择。